Homepage
Wasserionisierung durch Elektrolyse
- Zusammenfassung
- Historie der Wasserionisierung
- Diy-Elektrolysegerät
- Gebrauchsanleitung für Diy-Elektrolysegerät
- Subj. H2-Wirksamkeitsanzeichen
- Wasserstoffherstellung im Diy-Elektrolysegerät
- Vorteile des Diy-Elektrolysegerätes
Anwendungen für basisches + saures Wasser
- Basisches H2-Katholyt
- Wasserstoffgas im H2-Katholyt
- H2-Katholyt-Gesundheitswirkungen
- Wasserstoffgas-Gesundheitswirkungen
- Saure Anolyt-Chlordioxidlösung (A-CDL)
- Anwendungen von Katholyt, Anolyt und Anolyt-Chlordioxid (A-CDL)
- Kombi-Anwendung für Hygiene, Haushalt, Landwirtschaft
- Kombi-Anwendung für Wellness, Gesundheit
Vertiefende, technische Infos
- Wasserionisierer-Funktionsweise
- Was bedeuten pH- und ORP-Werte?
- pH- und ORP-Werte guter Wasserionisierer
Säure-Basen-Milieu
- FAQs Säure-Basen-Milieu
- Basische Speisen/Getränke
- Saure Speisen/Getränke
- Säurebildende Speisen/Getränke
- Rascher pH-Ausgleich
Säuren-Basen-Gleichgewichtsverschiebung
Säuremilieu und Mikrobenentwicklung
- Entstehung von Lebens-Urbausteine
- Mikrobenentwicklung je nach Körpermilieu (Pleomorphismus)
- Mikroben in basischem oder saurem Körpermilieu
Wasserstoffwasser (H2-Wasser mit Diy-Elektrolysegerät selbst herstellen
Effektivitäts-Vergleich mit speziellen HRW-(hydrogen-rich-water)Geräten
Inhaltsübersicht:
- Verschiedene Methoden der Wasserstoffanreicherung im Trinkwasser
- Wasserstoffgas durch chemische Reaktion (z.B. Magnesium)
- Wasserstoffanreicherung durch HRW-Maker
- Wasserstoffgas durch Wasserionisierer
- Optimale Kombination: Wasserionisierung mit Magnesiumzugabe
- Ist der H2-Wasserionisierer den HRW-Geräten überlegen?
- Geschmacksvergleich zwischen Wasserstoff-Wasser aus HRW oder 2-Kammerionisierer
- Welche Vorteile hat der Selbstbau-H2-Wasserionisierer gegenüber anderen Wasserionisierern?
- Beispiele für HRW-Geräte und ihre Wirkungen
Verschiedene Methoden der Wasserstoffanreicherung im Trinkwasser
Wasserstoffwasser, d.h. molekularer Wasserstoff (H2) in Wasser kann auf verschiedene Weise hergestellt werden, z.B. durch
- Begasung von Wasser mit separat hergestelltem H2 (Wasserstoffgas) 16
- chemische Reaktion von Wasser mit alkali-erdigen Metallen 15 z.B. durch Verwendung von Magnesium(chlorid) u.a. mineralischen (z.B. Calcium) und metallischen Zusätzen in einem Metall- oder Kunststoff-Stick. Mineralzusätze können Wasserstoffgas H2 ohne oder mit Elektrolyse erzeugen. [mehr hier]
- durch ein HRW-Gerät (Hydrogen-Rich-Water). Dies ist ein einzelliges Elektrolysegerät ohne Trennmembran zwischen den beiden Elektroden. (z.B. ein Wasserionisierer mit entfernter Trennmembrane). [mehr]
- durch 2-Kammer- oder Durchfluss-Wasserionisierer (mittels Elektrolyse). 14. H2 entsteht dabei in der Kathodenkammer, während Sauerstoff in der Anodenkammer entsteht. Kathode und Anode sind dabei durch eine ionendurchlässige Membrane getrennt. [mehr]
Die HRW-Geräte kombinieren meist die Elektrolyse mit chemischer Reaktion (bevorzugt mit Magnesiumverbindungen). Grundsätzlich können auch Wasserionisierer mit Magnesiumzusatz mehr Wasserstoff produzieren, aber für diesen Zweck müssten sie anders konzipiert sein. Mit einem leicht selbst und preiswert herstellbaren Diy-Elektrolysegerät lassen sich die Vorteile von chemischer Reaktion + HRW + Wasserionisierer kombinieren.
Wasserstoffgas durch chemische Reaktion
Seit ca. 2008 wurde der zuvor nur für elektrolytische Geräte verwendete Begriff Wasserionisierer" auf chemische Wasseraufbereitungsgeräte erweitert. Eine leichte, rasche und preiswerte Methode, H2-reiches Wasser zu erzeugen, besteht im Hinzufügen von alkalischem Erdmetall - zum Beispiel von Magnesiumchlorid. 15
Wenn z.B. Magnesiumstäbe (Sticks), 27 Magnesiumtabletten oder Magnesiumchloridpulver ins Wasser getan werden, dann produzieren sie im Wasser 7 rasch eine 2-4 ppm H2-Konzentration.
Es gibt auch Wasserfilter, die Magnesiummittel enthalten. 28
Magnesium reagiert mit Wasser und produziert H2-Gas ([Mg + 2H2O –> H2 + Mg(OH–)2]. Das Magnesium Hydroxid (Mg(OH–)2) zerfällt in Magnesiumionen (Mg2+ ) und Hydroxid Ionen (OH-) gemäß dem Gleichgewicht: Mg(OH–)2 <–> Mg2+ + 2OH– 24 Die Reaktion im Wasser ist nie so Hitze erzeugend, dass es eine Explosion erzeugen könnte.25
Diese chemische Methode zur H2-reichen Wasserproduktion ist bei Forschern für menschliche Studien beliebt, weil sie leicht zu nutzen ist. 13 Die Konzentration von molekularem Wasserstoffgas liegt generell nahe dem Sättigungspunkt (1.6 ppm),26. Das erlaubt dem Nutzer, größere Mengen des molekularen Hydrogens aufzunehmen ohne eine große Wassermenge dafür trinken zu müssen (1 Liter gegenüber 10 Litern)
Magnesium wurde in der Medizin schon lange gegen Übersäuerung, als Entspannungsmittel und für viele weitere gesundheitliche Zwecke gebraucht.
Wasserstoffanreicherung durch HRW-Maker
Seit im Jahre 2008 Shigeo Ohta eindeutig belegte, dass nicht das negative Redoxpotential von basischem Katholyt, sondern der Gehalt an molekularem Wasserstoffgas (H2) für dessen energetisierende und antioxidative Wirkung verantwortlich ist, entwickelt sich der Forschungsstand über den therapeutischen Nutzen von wasserstoffangereichertem Wasser (engl. HRW = hydrogen rich water) bemerkenswert rasch.
Kommerziell lösen inzwischen HRW-Geräte (Hydrogen-rich-water) die bisher so erfolgreichen Wasserionisierer zunehmend ab. HRW-Geräte sind meist kleiner, technisch einfacher und daher preiswerter als die meist recht großen, technisch teils sehr komplexen und teuren Wasserionisierer.
Vor allem Prof. Le Baron wirbt für Wasserstoffgas, das durch 1-Kammer-Elektrolyse ohne Trennmembrane gewonnen wird.
Technisch unterscheidet sich ein HRW-Gerät von einem Wasserinosierer vor allem dadurch, dass seine beiden Elektroden nur in einer Kammer Wasser elektrolysieren (= 1-Kammer-Elektrolyse), während im vergleichbaren 2-Kammer-Wasserionisierer die beiden Elektroden sich in 2 Kammern (2-Kammer-Elektrolyse) befinden, die durch eine halbdurchlässige Membran getrennt sind.
Das Wasser wird im HRW-Gerät sowohl mit Wasserstoff von der Kathode als auch zugleich mit Sauerstoff von der Anode angereichert. Es bleibt dabei pH-neutral. Die Anreicherung mit H2 und O2 geschieht im Verhältnis 2:1. Da sich neben H2aber auch O2 anreichert, welches das ORP wieder steigen lässt, kommt es nicht zur maximal möglichen Wasserstoffsättigung von 1,6 mg/Liter. Wenn Sauerstoff und Wasserstoff gleichzeitig durch das Wasser gasen, ändert sich das Redoxgleichgewicht je nachdem, welches Gas das Wasser schneller verlässt. Das wiederum hängt von der Zusammensetzung des Leitungswassers ab und davon, wie viel von den beiden und anderen Gasen bereits vor der Elektrolyse im Wasser gelöst waren. Meist entsteht dabei doppelt so viel Wasserstoffgas wie Sauerstoff.
Beispiele für HRW-Geräte s. Bild Susosu-Gerät oder BlueWater 700, Bildersammlung bei Google
Bei einem HRW-Gerät (bzw. einem Wasserionisierer mit entfernter Trennmembrane) wird das Wasser an der Kathode mit Wasserstoff und an der Anode mit Sauerstoff angereichert.
Sauerstoff ist der Gegenspieler von Wasserstoff und oxidativ, aber die Oxidation des Wasserstoffs findet in einem HRW-Gerät nicht sofort und nur über Umwege statt, sodass beide Gase einigermaßen stabil im Wasser getrennt bleiben und nicht zu Wasser reagieren. In der Anfangsphase ist nach wenigen Minuten der Elektrolyse meist mehr Wasserstoff im Wasser gelöst als Sauerstoff.
Dabei ändert sich das Redoxgleichgewicht je nachdem, welches Gas das Wasser schneller verlässt. Das wiederum hängt von der kompletten Zusammensetzung des Leitungswassers ab und davon, wie viel von den beiden und anderen Gasen bereits vor der Elektrolyse im Wasser gelöst waren.
HRW-Geräte würden aus dem Ausgangswasser ebenso viel bzw. ebenso wenig Wasserstoffgas erzeugen wie Wasserionisierer. Um möglichst rasch möglichst viel Wasserstoffgas zu erzeugen, wird in HRW-Geräten dem Wasser meist eine Magnesiumverbindung (z.B. Magnesiumcitrat, Magnesiumchlorat u.a. Mineralien) beigefügt. Mit dieser Kombination von Elektrolyse und chemisch-mineralischem Zusatz kann man preiswert, durchaus effektiv Wasserstoffgas mit ca. 0,8 mg/L herstellen.
Im Gegensatz zu fast allen Wasserionisierern ist in den HRW-Geräten entweder eine Mineralien-Zumischmöglichkeit vorgesehen bzw. wird dem Gerät gleich eine (Magnesium-)Mineralmischung fest oder flexibel zugefügt. Sie muss immer wieder erneuert werden, um wieder Wasserstoffgas produzieren zu können.
Wüßten die HRW-Gerätekäufer, dass sie lediglich ca. 1 Msp.sehr preiswertes Magnesiumchlorid auf 1 Liter Wasser benötigen, um eine gute Wasserstoffgas-Ausbeute zu bekommen, wären sie wohl kaum bereit, extrem überteuerte (Magnesium)Mineralmischungen zu bezahlen.
Wasserstoffgas durch Wasserionisierer
Bild: Wasserionisierer (Diy-Elektrolysegerät) mit V4A-Elektrode
Exakte Bauanleitung und viele Anwendungsmöglichkeiten werden ausführlich beschrieben in der Buchneuerscheinung (7/2023) von Gerd Gutemann: H2-Wasserionisierer selbst herstellen": Paperback, 208 Seiten, 16,99 , ISBN-13: 9783757812294, Verlag: Books on Demand, Erscheinungsdatum: 14.07.2023; Bestelladresse mit Leseprobe: https://www.bod.de/buchshop/h2-wasserionisierer-selbst-herstellen-gerd-gutemann-9783757812294 oder über den Buchhandel.
Kurzfassung der Wirkungen von Wasserstoffwasser und Anolyt aus dem Diy-Elektrolysegerät
1995 wurde gezeigt, dass reduzierendes, antioxidatives Wasser (Basisches Aktivwasser) ums 200- bis zum 500-fachen mit molekularem Wasserstoff (H2) angereichert werden kann im Vergleich zum Wasser vor der Elektrolyse. Hohe Wasserstoffgasbildung und negatives Reduktionspotential des basischen Wassers ist das Resultat der Produktion von atomarem und molekularem Wasserstoff in der Kathodenzelle.
In Japan wurde 1966 von Yoshimi Sano der erste Wasserionisierer" für Zuhause entwickelt. Damit kann man basisches (und saures) AktivWasser selbst herstellen. Basisches Wasser speichert Energie in Form von gelöstem Wasserstoffgas und wirkt antioxidativ, d.h. gegen freie Radikale.
Laien können H2-reiches Wasser am einfachsten und preiswertesten herstellen durch Wasserstoffanreicherung in einem Wasserionisierer mit Trennmembrane.Eine volle H2-Sättigung (1,6 mg/l) wird am sichersten erzielt, wenn der gelöste Sauerstoff aus dem Wasser entfernt wird. Dies geschieht nur im (Selbstbau)Wasserionisierer mit Trennmembrane, nie im HRW-Gerät.
Wasserionisierer produzieren Wasserstoffgas (H2) durch Elektrolyse. 17 Dies ist zugleich eine Methode zur Massenproduktion von molekularem Wasserstoffgas für die Energiegewinnung. 18. Die H2-Gaskonzentration durch Wasserionisierer variiert signifikant von weniger als 0.05 ppm auf bis zu 2.5 ppm. Dies hängt ab von der Wasserquelle, dem Magnesiumgehalt des Wassers, der Durchflussrate, Design und der Sauberkeit der Elektroden. Typischerweise ist bei Wasserdurchlaufionisierern bei normaler Flußgeschwindigkeit und normalem Wasser die Konzentration von H2 in der Kathodenkammer ca. 0.1ppm bis 0.7 ppm. 19-22 Läuft das Wasser sehr langsam durch, können diese Geräte zwar die molekulare H2-Konzentration ansteigen lassen, aber das resultierende pH ist sehr hoch und macht das Wasser ungenießbar. 22
Die Fähigkeit, hohe Konzentrationen von molekularem H2-Gas bei genießbarem pH (weniger als 9.5 oder neutral) zu erreichen, ist wichtig, wenn solche Geräte in Betracht gezogen werden. 21
Der Gehalt an gelöstem Wasserstoffgas H2 liegt bei einem guten (Durchfluss)ionisierer bei einem pH-Wert von 9 und Zimmertemperatur schon zwischen 1200 und 1300 Mikrogramm/l.
Trinken sollte man das Wasser nur bis zu einem pH Wert von 9.5, das bedeutet je nach Ionisierer Wasserstoffgas von 1250 bis 1450 Mikrogramm/l.
Wenn der Wasserionisierer noch höhere pH-Werte erzielen kann, etwa pH 11, ist auch ein H2-Wert von 1800 Mikrogramm (1,8 mg)/l möglich. Diese hohe Sättigung kann man z.B. zur Übertragung von Wasserstoffgas auf andere Lebensmittel nutzen. Da der Wasserstoff seine beiden Elektronen leicht abzugeben bereit ist, kommt es so zu einer Senkung des Redoxpotentials, das die Zunahme an Elektronenverfügbarkeit signalisiert.
Die meisten 2-Kammer- oder Durchfluss-Wasserionisierer wurden zu einer Zeit entwickelt, als die große therapeutische Wichtigkeit des molekularen Wasserstoffes noch unbekannt war. Sie wurden für die Herstellung von basischem oder saurem Wasser mit hohem und tiefem pH-Wert konzipiert, aber nicht für eine hohe gelöste H2-Konzentration.
Optimale Kombination: Wasserionisierung mit Magnesiumzugabe Um die Wasserstoffgasausbeute zu erhöhen und gleichzeitig die Produktionszeit zu verringern, kann man grundsätzlich zumindest bei 2-Kammer-Wasserionisierern dem Wasser (wie bei den HRW-Geräten üblich) ebenfalls eine Magnesiumverbindung (z.B. Magnesiumchlorid, Magnesiumcitrat oder Magnesiumchlorat) beifügen.
Das setzt voraus, dass beim Gerät eine Zumischung möglich ist. Das ist zwar bei den 2-Kammerionisierern der Fall, aber die relativ großen Kammern sind für eine hohe Wasserstoffgasproduktion nicht optimiert, weshalb der Prozess lange dauert. Nur bei ganz wenigen (= den teuersten) Durchfluss-Wasserionsierern könnte zwar Magnesium (statt einer Solemischung) zugefügt werden, aber dafür sind die Zumischkammern wieder überdimensioniert, und durch komplizierte Regelungsautomatik zu teuer...
Weder die 2-Kammer-Wasserionisierer noch die Wasserdurchflussionisierer wurden für optimale Wasserstoffgaserzeugung konstruiert, weil die therapeutische Bedeutung von Wasserstoffgas bis 2007 unbekannt war. Daher erweisen sie sich für die Wasserstoffherstellung i.A. als zu groß, zu kompliziert, technisch überzüchtet, zu pflegeaufwändig und insgesamt in Anschaffung und Unterhalt zu teuer. Daher verlieren sie im Wettbewerb mit HRW-Geräten zunehmend an Boden.
Der Selbstbau-H2-Wasserionisierer (Diy-Elektrolysegerät) ist jedoch so konzipiert, dass er die Vorteile der chemischen Wasserstoffgasbildung mit der physikalischen Wasserionisierung im 2-Kammer-Wasserionisierer-System mit Trennmembrane kombiniert.
Weil erst seit 2007 bekannt ist, dass hauptsächlich ein hoher Wasserstoffgas-Anteil im basischen Katholyt die gesundheitlichen Wirkungen hervorruft, wurden fast immer nur pH- und ORP-Messungen als eigentliche Leistungskriterien für den Gerätevertrieb hervorgehoben. Messungen zum Wasserstoffgas-Gehalt waren daher eine Ausnahme. Gerade sie sollten aber in Zukunft die ausschlaggebende Rolle spielen!
Ist der H2-Wasserionisierer den HRW-Geräten überlegen?
Folgende Vorteile weist der Selbstbau-H2-Wasserionisierer gegenüber den HRW-Geräten auf:
- Da er mit mehr Leistung (beliebig starke Gleichstromerzeugung) elektrolysieren kann, entsteht das Wasserstoffgas schneller und konzentrierter als in einem HRW-Gerät. K.H. Asenbaum konnte durch Vergleichsmessungen klar beweisen, dass ein (Einkammer-)HRW-Gerät nur die halbe Wasserstoffgas-Produktion eines 2-Kammer-Wasserionisierers erreicht.
- Die Art und Menge der Zumischung an Magnesiumchlorid, (Meer)Salz oder speziellen basischen Mineralien etc. kann je nach Zweck gewählt werden. Wasserstoffgas entsteht dadurch schon wenige Sekunden nach dem Elektrolysebeginn, wenn man eine ausreichend große Spannung (ich verwende ein 24 Volt., 2 A-Gerät) verwendet.
- Ersatz der Mineralienmischung ist leicht und preiswert erhältlich.
- die Wasserstoffkonzentration kann in der getrennten Kathodenkammer rascher und besser erfolgen, weil der Sauerstoff durch die Membrane in die Anodenkammer abwandert.
- weil der Wasserstoff im Kathodenwasser aufgrund der Abwanderung des Sauerstoffes keinen Sauerstoff-Redoxpartner mehr hat, bekommt das basische, hydrogenreiche Wasser ein sehr niedriges (negatives) Redoxpotential, das stark antioxidante Wirkungen gegen freie Wasserstoffradikale hat.
- Maximale Wasserstoffaufnahme durch Trinken während des Elektrolysevorganges aus der Kathodenkammer mittels Trinkhalm
- wegen der Trennmembran erfolgt keine Geschmacksvermischung der basischen und sauren Ionen. Das H2-Wasser schmeckt angenehm-leicht-süffig. Allerdings sollte es nicht mehr über pH 10 dauerhaft getrunken werden.
- der Geschmack des HRW-Wassers verändert sich im einkammerigen HRW-Gerät aufgrund der Vermischung mit chlorigen Ionen von der Anode, sobald die Elektrolyse (bei 24 V, 1 Msp. Magnesiumchlorid/L) über 30-40 Sekunden dauert. Danach wird der Geschmack immer chloriger und auch noch so wasserstoffreiches Wasser wird letzlich ungenießbar.
- Durch die Membrantrennung erfolgt eine klare Aufteilung in basisches, wasserstoffgasreiches Katholyt in der Kathodenkammer und saures Anolyt-Wasser in der Anodenkammer. Jedes Produkt hat seine eigenen nützlichen Anwendungsmöglichkeiten.
- Während HRW-Geräte hauptsächlich Wasserstoffwasser erzeugen, reichern Wasserionisierer im Katholyt außerdem noch andere, gesundheitlich wichtige basische Mineralien (Natrium, Kalium, Kalzium, Magnesium) an. Ionisiert sind sie leicht verwertbar und haben zusätzliche positive gesundheitliche Auswirkungen z.B. gegen Übersäuerung.
- Sobald ab ca. 45 Jahren der Basenpuffer Bikarbonat aus noch ungeklärten Gründen im Blut des Menschen abnimmt, entstehen mit dem Alter und der oft falschen Lebensweise Kur- und Übersäuerungskrankheiten (u.a. Diabetes, Bluthochdruck, Krebs). Diese sind mit basischem Wasser mit seinem höheren Mineralien- und Wasserstoffanteil wirksam zu behandeln.
Mehr zur HRW-Geräten im Vergleich zu Wasserionisierern: hier
Das basische, wasserstoffreiche Katholyt ist für viele therapeutische Zwecke nützlich.

Selbstbau-H2-Wasserionisierer mit gewellter Edelstahlelektrode. Trinkhalm zum Absaugen des Wasserstoffgases aus der Kathodenkammer
Geschmacksvergleich zwischen Wasserstoff-Wasser aus HRW oder 2-Kammerionisierer Entfernt man in einem 2-Kammer-Wasserionisierer die trennende Membrane, erfolgt die Elektrolyse auch nur noch in 1 Kammer (= HRW-Modus).
Tests mit dem Selbstbau-H2-Wasserionisierers bei 24 Volt Spannung und 1 Msp. Magnesiumchlorid in 1 Liter Wasser ergaben, dass mit und ohne Trennmembrane an der Kathodenelektrode Wasserstoffgas deutlich sichtbar zunahm, und an der Anode Sauerstoff entstand.
Das Wasser im HRW-1-Kammermodus ohne Trennmembran schmeckte allerdings nur neutral-angenehm, wenn es nur ca. 30 Sekunden elektrolysiert wurde. Wurde es länger elektrolysiert, änderte sich der Geschmack dahingehend, dass es ab ca. 45 Sekunden zunehmend chloriger schmeckte, weil die von der Anode ausströmenden chlorhaltigen und sauren Ionen das Wasser zum Genuss immer untauglicher machten. Nach ca. 90 Sekunden war das Wassergemisch trotz hohen Wasserstoffgasanteiles praktisch ungenießbar geworden, weil der Chlorgeschmack alles überdeckte.
Wurde unter denselben Bedingungen im 2-Kammer-Modus die Membrane zwischen die Elektroden gebracht, dann blieb der Wassergeschmack in der Kathodenkammer neutral-angenehm, solange nicht pH-Werte von über 10,5 erreicht wurden. Danach fing es an, seifig zu schmecken.
In der Anodenkammer konzentrierte sich der chlorig-saure Teil im 2-Kammer-Gerät, ohne geschmacklich auf das Wasserstoffwasser negativ einzuwirken.
Aus diesem Versuch lässt sich wohl ableiten, dass die preiswerteste und zugleich wohl effektivste Art, hochgesättigtes und wohlschmeckendes Wasserstoffgas herzustellen, im selbst leicht herstellbaren H2-Wasserionisierer erfolgt, wenn in dessen beide Kammern etwas Magnesiumchlorid ins Ausgangswasser zugefügt wird. Das dabei entstehende Wasserstoffwasser kann direkt während der Entstehung schon getrunken werden (= höchste H2-Konzentration dadurch).
Vorteile des Selbstbau-H2-Wasserionisierers (Diy-Elektrolysegerät)
Welche Vorteile hat der Selbstbau-H2-Wasserionisierer gegenüber anderen Wasserionisierern?
Weitere Vergleiche:
- dem Wasser können Mineralien (z.B. Sole, Magnesium etc.) zugefügt werden = raschere und stärkere Erzeugung von Wasserstoffgas = höhere pH-Werte
- die Wasserstoffgas-Bildung ist sehr rasch sichtbar
- Wasserstoffgas kann direkt mittels Trinkhalm aus der Kathodenkammer abgesaugt und getrunken werden = höchste Wasserstoffgas-Sättigung
- die Reinigung einer verkalkten Kathode kann durch das Anolyt aus der Anodenkammer leicht und kostenfrei erfolgen, benötigt also keine zusätzlichen Entkalkungsmittel (z.B. Zitronen- oder Essigsäure)
- preiswerte Eigenherstellung, Wartung, Reparatur, Ersatzteilaustuasch ist möglich
- Die Vorteile eines 2-Kammer-Wasserionisierers gegenüber Durchfluss-Wasserionisierern
- Spezielle Vorteile und Alleinstellungsmerkmale des Selbstbau-H2-Wasserionisierers
- Handhabung bei Herstellung und Anwendungen ist einfach, risikolos und sicher
Die Möglichkeit, das molekulare Wasserstoffgas H2 direkt aus der Kathodenkammer während der Entstehung trinken, ist bei den kommerziellen 2-Kammer-Wasserionisierern und den Durchlaufwasserionisierern (bislang m.W.) nicht möglich, weil m.W. alle kommerziellen 2-Kammer- oder Durchlaufwasserionisierer während des Elektrolyservorgangs dicht verschlossen sind oder keine Zumischmöglichkeit bieten! Dies ist ein entscheidender Vorteil des Diy-Gerätes gegenüber den kommerziellen Geräten!
Beispiele für HRW-Geräte und ihre Wirkungen
Quellennachweise
- 1 OHTA, S. (2012). Molecular hydrogen is a novel antioxidant to efficiently reduce oxidative stress with potential for the improvement of mitochondrial diseases. Biochimica et Biophysica Acta 1820, 586-94.
- 2 HUANG, C. S., KAWAMURA, T., PENG, X., TOCHIGI, N., SHIGEMURA, N., BILLIAR, T. R., NAKAO, A. & TOYODA, Y. (2011). Hydrogen inhalation reduced epithelial apoptosis in ventilator-induced lung injury via a mechanism involving nuclear factor-kappa B activation. Biochemical and Biophysical Research Communications 408, 253-8.
- 3 CHEN, H., SUN, Y. P., LI, Y., LIU, W. W., XIANG, H. G., FAN, L. Y., SUN, Q., XU, X. Y., CAI, J. M., RUAN, C. P., SU, N., YAN, R. L., SUN, X. J. & WANG, Q. (2010). Hydrogen-rich saline ameliorates the severity of L-arginine-induced acute pancreatitis in rats. Biochem Biophys Res Commun 393, 308-313.
- 4 OHARAZAWA, H., TSUTOMU IGARASHI, TAKASHI YOKOTA, HIROAKI FUJII, HISAHARU SUZUKI, MITSURU MACHIDE, HIROSHI TAKAHASHI, SHIGEO OHTA, AND IKUROH OHSAWA. (2010). Protection of the retina by rapid diffusion of hydrogen: administration of hydrogen-loaded eye drops in retinal ischemiareperfusion injury. Investigative ophthalmology & visual science 51, 487-492.
- 5 YOON, K. S., HUANG, X. Z., YOON, Y. S., KIM, S. K., SONG, S. B., CHANG, B. S., KIM, D. H. & LEE, K. J. (2011). Histological study on the effect of electrolyzed reduced water-bathing on UVB radiation-induced skin injury in hairless mice. Biological and Pharmaceutical Bulletin 34, 1671-7.
- 6 CHEN, X., ZHAI, X., KANG, Z. & SUN, X. (2012). Lactulose: an effective preventive and therapeutic option for ischemic stroke by production of hydrogen. Medical Gas Research 2, 3.
- 7 Sergej M. Ostojic The Effects of Hydrogen-rich Formulation for Treatment of Sport-related Soft Tissue Injuries http://clinicaltrials.gov/show/NCT01759498
- 8 GU, Y., HUANG, C. S., INOUE, T., YAMASHITA, T., ISHIDA, T., KANG, K. M. & NAKAO, A. (2010). Drinking Hydrogen Water Ameliorated Cognitive Impairment in Senescence-Accelerated Mice. Journal of Clinical Biochemistry and Nutrition 46, 269-276.
- 9 HUANG, C. S., KAWAMURA, T., TOYODA, Y. & NAKAO, A. (2010). Recent advances in hydrogen research as a therapeutic medical gas. Free Radical Research 44, 971-982.
- 10 ITO, M., HIRAYAMA, M., YAMAI, K., GOTO, S., ICHIHARA, M. & OHNO, K. (2012). Drinking hydrogen water and intermittent hydrogen gas exposure, but not lactulose or continuous hydrogen gas exposure, prevent 6-hydorxydopamine-induced Parkinson's disease in rats. Med Gas Res 2, 15.
- 11 CHRISTL, S. U., MURGATROYD, P. R., GIBSON, G. R. & CUMMINGS, J. H. (1992). Production, metabolism, and excretion of hydrogen in the large intestine. Gastroenterology 102, 1269-77.
- 12 Matsumoto, Akio, Megumi Yamafuji, Tomoko Tachibana, Yusaku Nakabeppu, Mami Noda, and Haruaki Nakaya. "Oral/hydrogen water/'induces neuroprotective ghrelin secretion in mice." Scientific reports 3 (2013)
- 13 OHNO, K., ITO, M. & ICHIHARA, M. (2012). Molecular hydrogen as an emerging therapeutic medical gas for neurodegenerative and other diseases. Oxidative Medicine and Cellular Longevity 2012, 353152.
- 14 SHIRAHATA, S., HAMASAKI, T. & TERUYA, K. (2012). Advanced research on the health benefit of reduced water. Trends in Food Science & Technology 23, 124-131.
- 15 NODA, K., TANAKA, Y., SHIGEMURA, N., KAWAMURA, T., WANG, Y., MASUTANI, K., SUN, X., TOYODA, Y., BERMUDEZ, C. A. & NAKAO, A. (2012). Hydrogen-supplemented drinking water protects cardiac allografts from inflammation-associated deterioration. Transpl Int 25, 1213-22.
- 16 GUO, J. D., LI, L., SHI, Y. M., WANG, H. D. & HOU, S. X. (2013). Hydrogen water consumption prevents osteopenia in ovariectomized rats. Br J Pharmacol 168, 1412-20.
- 17 Whitney, W. R. "Electrolysis of Water." The Journal of Physical Chemistry 7.3 (1903): 190-193.
- 18 ZENG, K. & ZHANG, D. K. (2010). Recent progress in alkaline water electrolysis for hydrogen production and applications. Progress in Energy and Combustion Science 36, 307-326.
- 19 FUJITA, R., TANAKA, Y., SAIHARA, Y., YAMAKITA, M., ANDO, D. & KOYAMA, K. (2011). Effect of molecular hydrogen saturated alkaline electrolyzed water on disuse muscle atrophy in gastrocnemius muscle. Journal of Physiological Anthropology 30, 195-201.
- 20 KIKUCHI, K., TAKEDA, H., RABOLT, B., OKAYA, T., OGUMI, Z., SAIHARA, Y. & NOGUCHI, H. (2001). Hydrogen particles and supersaturation in alkaline water from an Alkali-Ion-Water electrolyzer. Journal of Electroanalytical Chemistry 506, 22-27.
- 21 TANAKA, Y., UCHINASHI, S., SAIHARA, Y., KIKUCHI, K., OKAYA, T. & OGUMI, Z. (2003). Dissolution of hydrogen and the ratio of the dissolved hydrogen content to the produced hydrogen in electrolyzed water using SPE water electrolyzer. Electrochimica Acta 48, 4013-4019.
- 22 Testing performed by AquaSciences LLC
- 23 Chemistry (Zumdahl), 9th ed. P 932
- 24 Halka, M. (2010). Alkali & Alkaline-Earth Metals (Vol. 2). Infobase Publishing.
- 25 Jurs, Peter C. Chemistry: The molecular science. Vol. 2. Cengage Learning, 2008.
- 26 NAKAO, A., TOYODA, Y., SHARMA, P., EVANS, M. & GUTHRIE, N. (2010). Effectiveness of Hydrogen Rich Water on Antioxidant Status of Subjects with Potential Metabolic Syndrome-An Open Label Pilot Study. Journal of Clinical Biochemistry and Nutrition 46, 140-149.
- 27 KAJIYAMA, S., HASEGAWA, G., ASANO, M., HOSODA, H., FUKUI, M., NAKAMURA, N., KITAWAKI, J., IMAI, S., NAKANO, K., OHTA, M., ADACHI, T., OBAYASHI, H. & YOSHIKAWA, T. (2008). Supplementation of hydrogen-rich water improves lipid and glucose metabolism in patients with type 2 diabetes or impaired glucose tolerance. Nutrition Research 28, 137143.
- 28 /www.alkaway.com.au/products-ultrastream-water-alkaliser.html
Disclaimer: Die Beschreibung der Funktion des Selbstbau-Elektrolysegerätes und der damit herstellbaren Produkte (basisches Katholyt mit Wasserstoffgas H2, saures Anolyt und saure Anolyt-Chlordioxidlösung (A-CDL)) werden als unverbindliche Informationen nur zu Forschungszwecken veröffentlicht.
Für die Richtigkeit oder eine ausreichende Information zur Anwendung für Desinfektion, Haushalt, Landwirtschaft, Industrie oder für Hygiene, Wellness, Prophylaxe oder Krankheiten bei Pflanzen, Tieren oder Menschen kann keine Verantwortung übernommen werden.
In Deutschland gilt ionisiertes, basisches Wasser im Bereich zwischen pH 6.5 und 9.5 als 'Trinkwasser'. Die erwähnten Elektrolyseprodukte sind keine zugelassenen Lebensmittel, Hygieneprodukte oder Mittel im Sinne des AMG. Sie können daher aus rechtlichen Gründen lediglich für eigenverantwortete Selbstexperimente hergestellt und verwendet werden. Heilungsversprechen werden ausdrücklich nicht gegeben.
Diese Hinweise können und sollen keine ärztliche Diagnose oder Behandlung ersetzen, die bei entsprechenden Krankheiten in Anspruch genommen werden sollen. Verantwortung für die Anwendung oder Nichtanwendung des Inhaltes trägt jeder Nutzer selbst.
Da Ärzte oder Apotheker meist wenig oder gar keine Kenntnisse bzw. Erfahrungen mit den erwähnten Produkten besitzen, ist die produktübliche Empfehlung "Wegen Risiken und Nebenwirkungen fragen Sie Ihren Arzt oder Apotheker!" kaum realisierbar. Eigeninitiative, Eigenverantwortung für die Gesundheit, die Bereitschaft für Neues und gesundes Selbstvertrauen sind stattdessen gefragt.
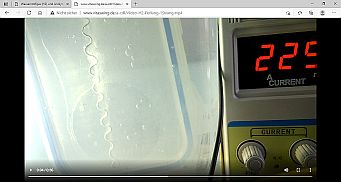
Foto links: Selbstbau-H2-Wasserionisierer mit gewellter V4A-Elektrode. Trinkhalm zum Absaugen/Abtrinken des Wasserstoffgases direkt an der Kathodenelektrode in der Mitte
Das Video zeigt, wie sofort nach dem Einschalten Wasserstoffgas (H2) direkt an der Elektrode gebildet wird und konzentriert sofort zur Wasseroberfläche strebt. Dort kann es unterhalb der Wasseroberfläche durch einen Trinkhalm (s. Bild links) sofort in außerordentlicher Konzentration abgesaugt und getrunken werden. Man kann es auch mit einer Spritze dort absaugen und in eine Flasche umfüllen. In einer Glasflasche bleibt das Wasserstoffgas nur wenige Stunden konzentriert, gast zunehmend aus. Man sollte das H2-Wasser daher möglichst frisch trinken!
Die Wasserkammer um die Kathode wird nur wenig mit Wasserstoffgas angereichert, sodass darin der pH-Wert nur langsam steigt und daher ca. 2-3 Minuten im Trinkwasserbereich bis pH 9,5 verbleibt. Damit gilt dieses hochgesättigte Wasserstoffgaswasser nach dt. Lebensmittelrecht noch als mineralisiertes 'Trinkwasser'.
Meine Telegramkanäle: Wasserstoffgas (H2): https://t.me/Wasserstoffgas_H2 | Anolyt-Chlordioxidlösung: https://t.me/A_CDL | Impfalternativen: https://t.me/impfalternativen | Prophezeiungen & Endzeitentwicklungen: https://t.me/Prophezeiungen
Home | Gesundheit | pH-Milieu | Diy-Elektrolysegerät
Bearbeitungsstand: 15.01.2026